提起“神经退行性疾病”,大家可能会比较陌生,但说到“阿尔茨海默症”,应该是无人不知。阿尔茨海默症(Alzheimer's disease, AD)又称早老性痴呆,是一种常见的神经退行性疾病。根据《2021年世界阿尔茨海默症报告》的数据,目前全球超过5500万人患有痴呆症;并且,这个数据仍在持续增长,预计到2030年痴呆症患者将达到7800万人[1]。
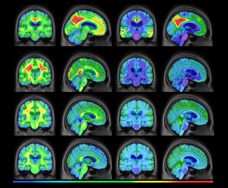
图1.《2021年世界阿尔茨海默症报告》封面[1]
https://www.alzint.org/u/World-Alzheimer-Report-2021.pdf
阿尔茨海默症(Alzheimer's disease, AD)又称早老性痴呆,是一种常见的神经退行性疾病。神经退行性疾病是由神经元及其髓鞘的进行性丧失导致的神经系统功能障碍,还包括帕金森病、癫痫、多发性硬化、肌萎缩性侧索硬化、脑损伤、亨廷顿病、Pick病以及不同类型的脊髓小脑共济失调等。神经退行性疾病的发生与年龄的增长成正相关,因此,在人口老龄化日益严重的今天,神经退行性疾病已成为全球性的重大公共卫生问题。近年来,针对该公共卫生问题的研究规模逐渐增大,研究层次也愈加深入,包括lncRNA在内的越来越多与神经退行性疾病相关的调节因子正逐步被发现。
lncRNA介绍
人类基因组中用于编码蛋白质的序列只占2.94%,而超过70%的基因组序列转录产生长非编码RNA(long noncoding RNA, lncRNA)。lncRNA是一类长度大于200 nt、且不具备蛋白质编码潜能的调控性RNA[2]。lncRNA广泛存在于各种生物体中,并且随着生物复杂度的增高,lncRNA对应的基因序列在基因组中所占的比例也越大。lncRNA通过多种效应模式广泛参与了对细胞活动的调节,并在大脑发育、神经元分化及功能维持等方面发挥了重要作用[3-4](图2)。
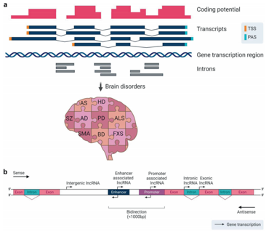
图2. lncRNA的示意图。
A:lncRNA对脑部疾病具有潜在影响。B:lncRNA可来源于内含子、外显子、基因间、增强子和启动子等区域。
lncRNA与神经退行性疾病
阿尔茨海默症(AD)
AD是最常见的神经退行性疾病,主要表现为个人记忆、语言、认知和运动机能的减退。典型的病理特征为出现细胞外老年斑(SPs)和细胞内神经纤维缠结(NFTs):SPs主要由β淀粉样蛋白(Aβ)组成,而NFTs则由tau蛋白的过度磷酸化引起。目前研究得比较清楚的AD相关长非编码RNA是 lncRNA 51A。lncRNA 51A是SORL1的反义转录本,研究表明,SORL1的下调可增强淀粉样病变,从而显著增加了阿尔茨海默症的患病风险。51A通过调节SORL1 pre-mRNA的剪接加工造成SORL1的变构体A减少,从而导致Aβ积累;并且,AD患者大脑皮层和血浆中51A水平明显升高,血浆51A可以作为判断AD进程的重要指标。
此外,NAT-Rad18、BDNF-AS、BC200等lncRNA也通过多种途径参与了AD的发生和发展。
帕金森病(Parkinson's disease,PD)
PD是仅次于阿尔茨海默症的全球第二大神经退行性疾病,同时也是最为常见的由神经功能障碍引起的运动障碍疾病。其关键机制是中脑黑质多巴胺能神经元的丧失,在路易体中发现的PD标志物α-突触核蛋白也被认为是PD的分子诱因。当前研究显示,lncRNA在PD的发生中同样起着重要作用。
1. UCHL1-as:UCHL1-as高表达于黑质纹状体和间脑,与泛素羧基末端水解酶L1 (UCHL1)的mRNA 5'端部分重叠,通过提供核糖体内部进入位点(IRES)增加UCHL1的翻译。
2. MAPT-as:微管相关蛋白tau(MAPT)在轴突细胞骨架稳定性中发挥作用,lncRNA MAPT-as是MAPT反义转录产物,可通过促进MAPT 启动子的DNA甲基化来下调MAPT 表达。MAPT-AS在PD衍生组织的四个脑区中表达显著降低,因此MAPT被认为是PD的治疗靶点。
此外,HOTAIR参与了中脑多巴胺神经元的自噬,NEAT1在PD患者外周血细胞中水平显著上调,AL049437和AK021630 lncRNA在PD患者的黑质组织中表达分别升高和降低。
亨廷顿氏舞蹈症(Huntington's disease,HD)
HD是一种常染色体显性遗传性神经退行性疾病,一般在中年发病,表现为舞蹈样动作,并随着病情进展逐渐丧失语言、行动、思考和吞咽等能力。HD主要由四号染色体上的Huntington基因变异引起:Huntington基因第一个外显子含有一段CAG 重复序列,编码多聚谷氨酰胺,而CAG重复序列的过度扩增会引起蛋白产物的多聚谷氨酰胺链延长,进而引起病变。lncRNA HTTAS是Huntington基因的反义转录本,可发生可变剪接,从而产生两种剪切变构体:HTTAS-v1和HTTAS-v2。研究发现HD患者的额叶皮质HTTAS-v1表达降低,导致Huntington基因的异常表达。此外, TUG1、NEAT、MEG3等lncRNA在HD患者的脑组织中也发生表达紊乱,但相关机制还有待进一步研究。
神经退行性疾病的发病机制复杂,截至目前,针对其开发的核酸药物屈指可数,而其中最成功的非Nusinersen(商品名Spinraza)莫属,lncRNA同样具有被开发成为神经退行性疾病药物的潜能。此外,lncRNA自身还可作为治疗靶点进行药物的设计和开发,比如针对神经退行性疾病相关的lncRNA,可采用比较成熟的RNA干扰或反义核酸等技术进行沉默和降解,也可通过小分子抑制剂识别并掩盖lncRNA与蛋白质的结合位点,或者通过小分子抑制剂与lncRNA结合,从而影响其正确折叠,使其构象发生改变,最终达到治疗疾病的目的。由于lncRNA具有多样化的生物学特征和功能,相信随着神经退行性疾病相关信号通路和分子机制的深入研究,治疗神经退行性疾病的lncRNA药物的出现指日可待。
参考文献:
1. Gauthier S, Rosa-Neto P, Morais JA, & Webster C. 2021. World Alzheimer Report 2021: Journey through the diagnosis of dementia. London, England: Alzheimer’s Disease International. https://www.alzint.org/u/World-Alzheimer-Report-2021.pdf
2. Winkle, M., El-Daly, S.M., Fabbri, M. et al. Noncoding RNA therapeutics-challenges and potential solutions. Nat Rev Drug Discov. https://doi.org/10.1038/s41573-021-00219-z
3. Yang S, Lim KH, Kim SH, Joo JY. Molecular landscape of long noncoding RNAs in brain disorders. Mol Psychiatry. https://doi.org/10.1038/s41380-020-00947-5
4. Li L, Miao H, Chang Y, Yao H, Zhao Y, Wu F, Song X. Seminars in Cancer Biology, Multidimensional crosstalk between RNA-binding proteins and noncoding RNAs in cancer biology. https://doi.org/10.1016/j.semcancer.2021.03.007


